insuline biogénétique humaine
FORMES et PRÉSENTATIONS |
Umuline Rapide, 100 UI/ml :
Solution injectable (aqueuse stérile, limpide, incolore) :
Cartouches de 3 ml, boîte de 5. A utiliser avec un stylo injecteur compatible, avec marquage CE.Flacon de 10 ml à utiliser avec une seringue appropriée marquée 100 UI/ml. Umuline NPH, 100 UI/ml :
Suspension injectable (stérile, formée d’un précipité blanc cristallisé) :
Cartouches de 3 ml, boîte de 5. A utiliser avec un stylo injecteur compatible, avec marquage CE.Flacon de 10 ml à utiliser avec une seringue appropriée marquée 100 UI/ml.
Umuline NPH Pen, 100 UI/ml :
Suspension injectable (stérile, formée d’un précipité blanc cristallisé) : Cartouches de 3 ml en stylo injecteur prérempli multidose jetable, boîte de 5.
Umuline Profil 30, 100 UI/ml :
Suspension injectable (stérile) :
Cartouches de 3 ml, boîte de 5. A utiliser avec un stylo injecteur compatible, avec marquage CE.Flacon de 10 ml à utiliser avec une seringue appropriée marquée 100 UI/ml.
Umuline Profil 30 Pen, 100 UI/ml :
Suspension injectable (stérile) : Cartouches de 3 ml en stylo injecteur prérempli multidose jetable, boîte de 5.
COMPOSITION |
| Umuline Rapide : | |
| Cartouche : | p cartouche |
| Insuline* soluble | 300 UI |
| Flacon : | p flacon |
| Insuline* soluble | 1000 UI |
Umuline Rapide est une préparation d’insuline d’action rapide.
| Umuline NPH et NPH Pen : | |
| Cartouche ou stylo : | p cart/p stylo |
| Insuline* isophane** | 300 UI |
| Flacon : | p flacon |
| Insuline* isophane** | 1000 UI |
Umuline NPH et NPH Pen sont des préparations d’insuline d’action intermédiaire.
Umuline NPH Pen délivre jusqu’à 60 unités en une dose et par paliers de 1 unité.
| Umuline Profil 30 et Profil 30 Pen : | |
| Cartouche ou stylo : | p cart/p stylo |
| Insuline* isophane**, biphasique | 300 UI |
| Quantité correspondant à : | |
| Insuline soluble | 90 UI |
| Insuline isophane | 210 UI |
| Flacon : | p flacon |
| Insuline* isophane**, biphasique | 1000 UI |
| Quantité correspondant à : | |
| Insuline soluble | 300 UI |
| Insuline isophane | 700 UI |
Suspension stérile d’insuline humaine composée de 30 % d’insuline soluble pour 70 % d’insuline isophane.
Umuline Profil 30 et Profil 30 Pen sont des préparations d’insuline d’action intermédiaire.
Umuline Profil 30 Pen délivre jusqu’à 60 unités en une dose et par paliers de 1 unité.
* insuline humaine produite dans Escherichia coli par la technique de l’ADN recombinant
** dans un tampon phosphate
INDICATIONS |
POSOLOGIE ET MODE D’ADMINISTRATION |
CONTRE-INDICATIONS |
- Hypoglycémie.
- Hypersensibilité à Umuline ou à l’un de ses composants, sauf dans le cadre d’un programme de désensibilisation.
- Les préparations d’Umuline ne doivent en aucun cas être administrées par voie intraveineuse, à l’exception d’Umuline Rapide (insuline soluble).
MISES EN GARDE et PRÉCAUTIONS D’EMPLOI |
- Le transfert à un autre type d’insuline ou à une autre marque chez un patient doit se faire sous strict contrôle médical. Le changement de concentration, de marque (fabricant), de type (Rapide, NPH, Profil), d’espèce (animale, humaine, analogue de l’insuline humaine) et/ou de méthode de fabrication (ADN recombinant versus l’insuline d’origine animale) peut nécessiter une modification de posologie.
- Les patients recevant de l’insuline humaine peuvent nécessiter un changement de posologie par rapport à leurs insulines d’origine animale. Si une adaptation posologique est nécessaire, elle peut être faite lors de la première administration ou au cours des premières semaines ou des premiers mois.
- Quelques patients ayant présenté des réactions hypoglycémiques après transfert d’une insuline d’origine animale à une insuline humaine ont signalé que les symptômes précurseurs d’hypoglycémie étaient moins prononcés ou différents de ceux ressentis lors de leur traitement antérieur par l’insuline animale. Les patients dont la glycémie s’est améliorée de façon importante, par exemple grâce à l’insulinothérapie intensifiée, peuvent voir disparaître certains ou tous les symptômes précurseurs d’hypoglycémie et doivent donc en être informés. La modification ou la diminution des symptômes précurseurs d’hypoglycémie peut également survenir chez les patients présentant un diabète de longue durée, une neuropathie diabétique ou prenant simultanément d’autres médicaments tels que les bêtabloquants. L’hypoglycémie non corrigée ou les réactions d’hyperglycémie peuvent entraîner une perte de connaissance, un coma ou le décès.
- L’utilisation de posologies mal adaptées ou l’arrêt du traitement, en particulier chez les diabétiques insulinodépendants, peut entraîner une hyperglycémie et une acidocétose diabétique dont le pronostic peut être fatal.
- Le traitement par insuline humaine peut provoquer la formation d’anticorps, mais leurs taux sont inférieurs à ceux observés avec l’insuline animale purifiée.
- Les besoins en insuline peuvent changer de façon significative en cas de maladies surrénalienne, hypophysaire ou thyroïdienne et d’insuffisance rénale ou hépatique.
- Les besoins en insuline peuvent augmenter au cours d’une maladie ou de perturbations affectives.
- L’adaptation posologique peut être nécessaire si le patient modifie l’intensité de son activité physique ou modifie son régime alimentaire habituel.
INTERACTIONS |
- Un certain nombre de médicaments sont connus pour interagir avec le métabolisme du glucose. Le médecin doit considérer toute possibilité d’interaction et demander aux patients s’ils prennent d’autres médicaments.
- Les besoins en insuline peuvent être augmentés par les substances à effet hyperglycémiant, telles que les glucocorticoïdes, les hormones thyroïdiennes, l’hormone de croissance, le danazol, les bêta-2 mimétiques (tels que ritodrine, salbutamol, terbutaline), les thiazidiques.
- Les besoins en insuline peuvent être diminués en présence de substances à effet hypoglycémiant, telles que les hypoglycémiants oraux (ADO), les salicylés (par exemple l’acide acétylsalicylique), certains antidépresseurs (les inhibiteurs de la monoamine oxydase : IMAO), certains inhibiteurs de l’enzyme de conversion (IEC) de l’angiotensine (captopril, énalapril), les antagonistes des récepteurs de l’angiotensine II, les agents bêtabloquants non sélectifs et l’alcool.
- Les analogues des somatostatines (octréotide, lanréotide) peuvent réduire ou accroître les besoins en insuline.
GROSSESSE et ALLAITEMENT |
CONDUITE et UTILISATION DE MACHINES |
EFFETS INDÉSIRABLES |
SURDOSAGE |
PHARMACODYNAMIE |
- Umuline Rapide : Insuline humaine d’action rapide (code ATC : A10AB01).
- Umuline NPH et NPH Pen : Insuline humaine d’action intermédiaire (code ATC : A10AC01).
- Umuline Profil 30 et Profil 30 Pen : Insuline humaine d’action intermédiaire (code ATC : A10AD01).
L’activité principale de l’insuline est la régulation du métabolisme glucidique.
D’autre part, l’insuline possède plusieurs actions anaboliques et anticataboliques dans différents tissus. Dans le muscle, ces effets comprennent une augmentation de la synthèse du glycogène, des acides gras, du glycérol, des protéines et une augmentation de la fixation des acides aminés, ainsi qu’une diminution de la glycogénolyse, de la néoglucogenèse, de la cétogenèse, de la lipolyse, du catabolisme protéique et de l’élimination des acides aminés.
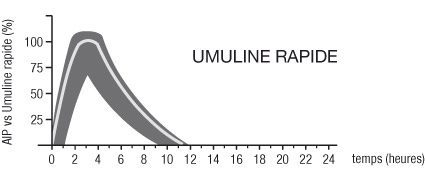
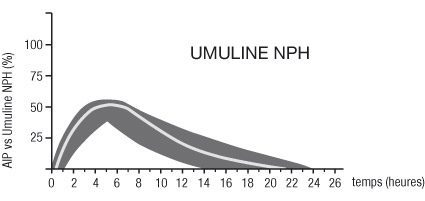
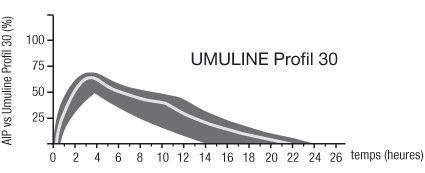
Les profils d’activité type (courbe d’utilisation du glucose) après injection sous-cutanée sont représentés sur les courbes ci-dessous par la ligne épaisse. Les variations en durée et/ou en intensité d’activité de l’insuline chez les patients sont représentées par la zone sombre.
La variabilité individuelle dépend de facteurs tels que la dose, le site d’injection, la température et l’activité physique du patient.
 |
 |
 |
PHARMACOCINÉTIQUE |
La pharmacocinétique de l’insuline ne constitue pas un reflet de l’action métabolique de cette hormone. Il est donc plus approprié d’examiner les courbes correspondant à l’utilisation du glucose (cf ci-dessus) afin de déterminer l’activité de l’insuline.
SÉCURITE PRÉCLINIQUE |
Umuline est une insuline humaine obtenue par la technologie d’ADN recombinant. Aucun effet secondaire grave n’a été observé lors des études de toxicité subchronique et aucun effet mutagène n’a été mis en évidence dans une série de tests de génotoxicité réalisés in vitro et in vivo.
INCOMPATIBILITÉS |
Les préparations d’Umuline ne doivent pas être mélangées avec des insulines produites par d’autres fabricants ou avec des préparations d’insuline d’origine animale.
CONDITIONS DE CONSERVATION |
A conserver au réfrigérateur (entre + 2 °C et + 8 °C).
Ne pas congeler. Ne pas exposer à une chaleur excessive ou au soleil.
Conserver le conditionnement primaire dans l’emballage extérieur.
- Après la première utilisation :
- Les cartouches, les flacons ou les stylos préremplis peuvent être utilisés pendant 28 jours. Ne pas utiliser au-delà de cette période.
- En cours d’utilisation :
- Les cartouches, les flacons ou les stylos préremplis doivent être conservés à une température ne dépassant pas + 30 °C.
MODALITÉS MANIPULATION/ÉLIMINATION |
- Préparation d’une dose :
-
- Umuline Rapide (solution) :
- Les cartouches et les flacons contenant Umuline Rapide ne nécessitent pas de remise en suspension et ne doivent être utilisés que si la solution est limpide, incolore, sans particules visibles et si elle a l’aspect de l’eau.
-
- Umuline NPH et Umuline Profil 30 (suspensions) :
- Immédiatement avant utilisation :
- cartouches et stylos préremplis : les faire rouler 10 fois entre la paume des mains, puis les retourner 10 fois à 180° ;
- flacons : les faire rouler plusieurs fois entre la paume des mains,
- cartouches et stylos préremplis : les faire rouler 10 fois entre la paume des mains, puis les retourner 10 fois à 180° ;
- afin de remettre l’insuline en suspension, jusqu’à ce qu’elle prenne un aspect uniformément trouble ou laiteux.
- Si cet aspect n’est pas obtenu, répéter la procédure ci-dessus jusqu’à ce que le contenu de la cartouche ou du flacon soit bien mélangé. Les cartouches contiennent une petite bille de verre pour faciliter le mélange. Ne pas agiter vigoureusement, car la formation d’une mousse pourrait gêner la mesure exacte de la dose.
- Examiner les cartouches et les flacons régulièrement et ne pas les utiliser si la suspension présente des floculations ou si des particules blanches restent collées au fond ou sur les parois de la cartouche ou du flacon, lui donnant un aspect givré.
-
- Mélange d’insulines :
-
- Flacons (Rapide et NPH) :
Commencer par aspirer l’insuline à action rapide dans la seringue, afin d’éviter la contamination du flacon par la préparation à durée d’action plus longue. Il est conseillé de réaliser l’injection immédiatement après le mélange. Toutefois, si un délai est nécessaire, procéder toujours de la même façon. - Il est également possible d’utiliser des seringues distinctes d’Umuline Rapide et d’Umuline NPH pour administrer la quantité requise de chaque préparation.
- Flacons (Rapide et NPH) :
-
- Cartouches et stylos préremplis :
Les cartouches ne sont pas conçues pour la réalisation d’un mélange avec d’autres insulines. Les cartouches vides ne peuvent être réutilisées.
- Cartouches et stylos préremplis :
-
- Cartouches :
- Les instructions particulières du fabricant pour chaque stylo injecteur doivent être suivies pour charger la cartouche, fixer l’aiguille et pratiquer l’injection d’insuline.
-
- Stylos préremplis :
- Suivre les instructions du stylo pour fixer l’aiguille et pratiquer l’injection d’insuline.
- Une aiguille doit toujours être fixée sur le stylo avant de purger, sélectionner et injecter la dose d’insuline.
- Le stylo prérempli doit toujours être purgé avant chaque injection. Ne pas purger le stylo peut entraîner une imprécision de dose.
-
- Flacons :
- Préparer la seringue avant l’injection, en suivant les instructions du médecin ou de l’infirmier.
- Utiliser une seringue à insuline graduée, adaptée à la concentration de l’insuline à administrer.
- Injection d’une dose :
- Injecter la dose correcte d’insuline en suivant les instructions du médecin ou de l’infirmier.
- Les points d’injection doivent varier afin de ne pas utiliser le même point d’injection plus d’une fois par mois environ.
- Chaque boîte contient une notice d’information contenant des instructions pour pratiquer l’injection d’insuline.
- Élimination des récipients et des aiguilles usagés :
- N’utiliser les aiguilles qu’une fois. Les jeter de manière à ne pas provoquer d’accident. Les aiguilles et les stylos ne doivent pas être partagés. Les cartouches, les flacons ou les stylos préremplis peuvent être utilisés jusqu’à ce qu’ils soient vides, puis doivent être convenablement jetés. Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM | 3400934038563 (1996) cart Umuline Rapide. |
| 3400933523664 (1992) fl Umuline Rapide. | |
| 3400934038792 (1996) cart Umuline NPH. | |
| 3400933523435 (1992) fl Umuline NPH. | |
| 3400934878824 (1998) Umuline NPH Pen. | |
| 3400934039454 (1996) cart Umuline Profil 30. | |
| 3400933523084 (1992) fl Umuline Profil 30. | |
| 3400934878244 (1998) Umuline Profil 30 Pen. | |
| AMM révisées le 10.08.2009. | |
| Prix : | 36.17 euros (5 cartouches Umuline Rapide). |
| 21.65 euros (flacon 10 ml Umuline Rapide). | |
| 36.17 euros (5 cartouches Umuline NPH). | |
| 21.65 euros (flacon 10 ml Umuline NPH). | |
| 40.69 euros (5 stylos Umuline NPH Pen). | |
| 36.17 euros (5 cartouches Umuline Profil 30). | |
| 21.65 euros (flacon 10 ml Umuline Profil 30). | |
| 40.69 euros (5 stylos Umuline Profil 30 Pen). | |
| Remb Séc soc à 65 %. Collect. | |
LILLY FRANCE SAS
13, rue Pagès. 92158 Suresnes cdx
Standard : Tél : 01 55 49 34 34
Info médic/Pharmacovigilance :
Tél : 01 55 49 32 51 ou N° Vert : 08 00 00 36 36
Fax : 01 55 49 33 07
Logistique produits :
Tél : 01 55 49 33 21. Fax : 01 55 49 34 85
Site web : http://www.lilly.fr
Liste Des Sections Les Plus Importantes :
- pathologies
- Medicaments
- Medicaments injectables
- Traitement D’Urgence
- Guide Infirmier Des Examens De Laboratoire
- Infirmiers En Urgences
- Fiche Technique Medical
- Techniques De Manipulations En Radiologie Medicale
- Bibliotheque_medicale



