salbutamol
Poudre (blanche) pour inhalation à 100 µg/dose :
Cartouche de 200 doses + inhalateur, boîte unitaire.Recharge de 200 doses, boîte unitaire.
| | p dose |
Salbutamol (DCI)
| 100 µg |
| (sous forme de sulfate : 120 µg/dose) |
Excipient : lactose monohydraté.
La quantité de principe actif dans la dose délivrée (à la sortie de l’embout buccal) est la même que la dose mesurée (à la sortie du compartiment doseur).
- Traitement symptomatique des maladies respiratoires obstructives réversibles, telles que l’asthme ou la bronchopneumopathie chronique obstructive à composante réversible.
-
- Prévention de l’asthme déclenché par l’effort ou par l’exposition aux allergènes.
-
POSOLOGIE ET MODE D’ADMINISTRATION
|
Posologie :
La dose préconisée dépend de la sévérité de la maladie et sera adaptée en fonction de l’évolution de l’état clinique du patient.
-
Adulte (y compris sujet âgé et adolescent) :
- Traitement symptomatique : une inhalation (soit 100 µg) à renouveler si besoin.
- Prévention de l’asthme déclenché par l’effort ou par les allergènes : deux inhalations (soit 200 µg) 10 à 15 minutes avant l’exercice ou l’exposition aux allergènes incriminés.
- La dose usuelle quotidienne ne devra pas dépasser 8 inhalations (soit 800 µg/24 h).
-
Enfant (de 6 à 12 ans) :
- Traitement symptomatique : une inhalation (soit 100 µg) à renouveler si besoin.
- Prévention de l’asthme déclenché par l’effort ou par les allergènes : une inhalation (soit 100 µg), à renouveler si besoin (soit 200 µg au total), 10 à 15 minutes avant l’exercice ou avant l’exposition aux allergènes incriminés.
- La dose usuelle quotidienne ne devra pas dépasser 4 inhalations (soit 400 µg/24 h).
-
Recommandations générales :
- Une inhalation peut apporter une amélioration rapide lors des épisodes de dyspnée aiguë ou de sibilants. Une deuxième inhalation peut être nécessaire dans les 5 à 10 minutes suivantes si les symptômes persistent. Chaque prise (de une ou deux inhalations) sera espacée d’au moins quatre heures.
- Si les symptômes persistent après la deuxième inhalation ou si l’état clinique du patient ne lui permet pas d’inspirer suffisamment dans le dispositif pour déclencher la libération de la poudre, une consultation médicale rapide est nécessaire. Si les bêta-2 mimétiques sont utilisés quotidiennement pour traiter les symptômes, une corticothérapie inhalée de fond devra être envisagée.
- L’utilisation fréquente de doses supérieures aux doses maximales recommandées ou une augmentation rapide de la consommation en bronchodilatateurs témoignent d’un contrôle insuffisant de la maladie ou d’une aggravation de l’asthme.
- Lorsqu’un autre dispositif d’inhalation est utilisé en remplacement de Ventilastin Novolizer, la quantité de principe actif distribué au poumon peut être différente, ce qui peut entraîner un réajustement de la posologie.
Mode d’administration :
Voie inhalée.
Un intervalle d’au moins une minute doit être respecté entre chaque inhalation.
-
Utilisation et manipulation du dispositif Novolizer :
-
| Dispositif Novolizer : |
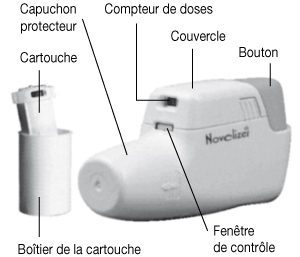 |
-
-
Rechargement :
-
- Appuyer légèrement sur les surfaces nervurées situées des deux côtés du couvercle, pousser le couvercle vers l’avant et le retirer.
-
- Retirer le film protecteur en aluminium du boîtier de la cartouche et prélever une cartouche neuve.
-
- Insérer la cartouche dans le Novolizer en orientant le compteur de doses face à l’embout buccal.
-
- Replacer le couvercle dans ses guides latéraux et le pousser horizontalement vers le bouton jusqu’à ce qu’il s’insère dans son logement. La cartouche peut être laissée dans le Novolizer jusqu’à ce qu’elle soit vide ou pendant trois mois au maximum après son insertion.
-
- Remarque : les cartouches de Ventilastin Novolizer ne peuvent être utilisées qu’avec le dispositif inhalateur de poudre Novolizer.
-
-
Mode d’emploi du dispositif :
-
- Toujours tenir le dispositif Novolizer horizontalement lors de son utilisation. Tout d’abord, retirer le capuchon protecteur.
-
- Appuyer à fond sur le bouton bleu. On perçoit alors un double déclic sonore et la couleur de la fenêtre de contrôle (en bas) passe du rouge au vert. Relâcher ensuite le bouton bleu. La couleur verte de la fenêtre indique que le Novolizer est prêt à l’emploi.
-
- Expirer (hors de l’inhalateur de poudre).
-
- Fermer les lèvres autour de l’embout buccal. Inhaler la poudre par une inspiration rapide et profonde. Pendant cette inhalation, on doit entendre un déclic sonore témoin d’une inhalation correctement effectuée. Retenir sa respiration pendant quelques secondes, puis respirer normalement.
- Remarque : si le patient a besoin de plusieurs inhalations, répéter les étapes 2 à 4.
-
- Replacer le capuchon protecteur sur l’embout buccal ; l’inhalation est maintenant terminée.
-
- Le chiffre qui apparaît dans la fenêtre supérieure indique le nombre de doses restantes, de 20 en 20 jusqu’à 60 doses restantes, et de 10 en 10 de 60 à 0 doses restantes.
- Remarque : il ne faut appuyer sur le bouton bleu qu’immédiatement avant l’inhalation.
-
- Avec le dispositif Novolizer, l’inhalation involontaire d’une double dose n’est pas possible. Le déclic sonore et le changement de couleur de la fenêtre de contrôle indiquent que l’inhalation a été effectuée correctement. Si la couleur de la fenêtre de contrôle demeure inchangée, il faut recommencer l’inhalation. Si l’inhalation n’est pas effectuée correctement après plusieurs tentatives, le patient devra consulter son médecin.
-
-
Nettoyage :
- Le dispositif Novolizer doit être nettoyé à intervalles réguliers et au minimum lors de chaque changement de cartouche. Pour connaître les instructions pour le nettoyage de l’appareil, se référer à la notice d’utilisation contenue dans la boîte.
- Remarque : afin d’assurer une utilisation correcte de l’inhalateur, il convient d’expliquer soigneusement au patient le mode d’emploi de l’appareil. Pour l’utilisation de ce médicament chez l’enfant, il conviendra de s’assurer qu’un adulte surveille l’administration du médicament.
Hypersensibilité (allergie) au principe actif (salbutamol) ou à l’un des excipients (cf Composition).
MISES EN GARDE et PRÉCAUTIONS D’EMPLOI
|
Le traitement de l’asthme sera adapté par palier en fonction de la sévérité.
Les bronchodilatateurs ne doivent pas être utilisés seuls pour le traitement de l’asthme modéré à sévère ou en cas d’asthme instable. Les patients atteints d’asthme sévère sont particulièrement exposés au risque de crise d’asthme aiguë grave pouvant menacer le pronostic vital et doivent donc être suivi régulièrement pour adaptation du traitement.
Le traitement par Ventilastin Novolizer 100 microgrammes/dose, poudre pour inhalation ne doit pas retarder la mise en route d’un traitement de fond régulier par corticoïdes inhalés s’il s’avère nécessaire.
Le salbutamol doit être utilisé avec prudence dans les cas suivants :
- Troubles cardiaques sévères, notamment infarctus du myocarde récent.
-
- Coronaropathie, cardiomyopathie obstructive et tachyarythmie.
-
- Hypertension artérielle sévère non contrôlée.
-
- Anévrisme.
-
- Hyperthyroïdie.
-
- Diabète mal contrôlé.
-
- Phéochromocytome.
-
Une auto-évaluation quotidienne des symptômes par le patient contribue au suivi de l’évolution de l’asthme et permet d’en vérifier son contrôle pour faciliter l’adaptation des traitements bronchodilatateur et anti-inflammatoire. Le médecin devra s’assurer que les patients sont formés à la réalisation de mesures régulières du débit expiratoire de pointe (DEP) au moyen d’un débitmètre de pointe portable.
Si l’asthme n’est pas suffisamment contrôlé ou se détériore, ou bien si le patient augmente sa consommation de bronchodilatateurs par voie inhalée pour traiter ses symptômes, une consultation médicale est nécessaire afin de réévaluer la conduite thérapeutique. Il convient alors d’envisager la mise en route ou l’augmentation de la corticothérapie inhalée voire l’instauration d’une corticothérapie orale en cure courte. L’augmentation des prises des bronchodilatateurs, et en particulier d’un bêta-2 stimulant à action rapide et brève, pour soulager les symptômes reflète une détérioration de l’asthme. Si un patient développe en quelques jours une augmentation rapide des symptômes on doit craindre une décompensation de sa maladie et la possibilité d’une évolution vers un état de mal asthmatique. Le patient devra être informé que dans ces conditions il convient de consulter rapidement un médecin.
Si la dose habituellement efficace de béta-2 mimétiques à action rapide et de courte durée devient insuffisante ou si l’augmentation de la fréquence de ses symptômes nécessitent une augmentation de la consommation de bronchodilatateurs, un avis médical est nécessaire pour réévaluer la conduite thérapeutique. Des doses supérieures aux doses recommandées sont susceptibles de favoriser l’apparition des effets indésirables sévères tels que troubles cardiaques, hypokaliémie, altération du goût, nausées, agitation, hypersudation, céphalées, tremblements.
Les bêta-2 stimulants peuvent induire une hypokaliémie potentiellement grave, s’ils sont administrés par voie parentérale ou par nébulisation. La prudence est recommandée en cas d’asthme aigu grave car les effets hypokaliémiants peuvent être potentialisés par l’hypoxie ou l’administration concomitante de dérivés xanthiques, stéroïdes ou de diurétiques. Dans ces situations, la surveillance de la kaliémie est recommandée.
Le salbutamol à forte dose par voie inhalée peut induire une augmentation de la glycémie. Une surveillance étroite de la glycémie est donc recommandée chez les patients diabétiques.
Les produits à base de salbutamol destinés à être administrés par voie inhalée sont inadaptés pour le traitement des menaces d’accouchement prématuré.
Le lactose peut contenir des traces de protéines de lait. La quantité de lactose contenue dans Ventilastin n’induit normalement pas de trouble chez les sujets intolérants au lactose.
Il conviendra d’expliquer au patient le mode d’utilisation du dispositif Novolizer et de vérifier sa technique d’inhalation pour s’assurer de son aptitude à utiliser correctement le dispositif Novolizer.
L’attention des sportifs sera attirée sur le fait que cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Interactions médicamenteuses :
- Le salbutamol et les bêtabloquants non sélectifs ne doivent généralement pas être associés. L’administration d’un bêtabloquant chez un asthmatique l’expose à un risque de bronchoconstriction sévère.
-
- L’administration concomitante de salbutamol et d’anesthésiques halogénés (tels que halothane, méthoxyflurane ou enflurane) augmente le risque de survenue de troubles du rythme et d’hypotension sévères. En prévision d’une anesthésie, les prises de salbutamol devront être interrompues au moins 6 heures avant l’administration d’un anesthésique halogéné.
-
- Le traitement par salbutamol peut entraîner une hypokaliémie (cf Mises en garde/Précautions d’emploi et Effets indésirables). Cet effet peut être potentialisé par l’administration concomitante d’autres médicaments, notamment les xanthines, glucocorticoïdes, diurétiques et glucosides cardiotoniques (digoxine). Il est recommandé de surveiller la kaliémie si ces traitements sont associés.
-
- Les inhibiteurs de la monoamine oxydase et les antidépresseurs tricycliques peuvent augmenter le risque d’effets indésirables cardiovasculaires.
-
Les études précliniques et une expérience clinique de longue durée n’ont pas révélé d’effets tératogènes du salbutamol. Une augmentation de la fréquence cardiaque peut être observée chez le foetus lors de l’administration de salbutamol chez la femme enceinte.
Le salbutamol est excrété dans le lait maternel, et l’administration de fortes doses peut entraîner la survenue d’effets pharmacologiques chez l’enfant au cours de l’allaitement.
Le salbutamol reste le traitement bronchodilatateur de première intention chez la femme enceinte. Néanmoins, son administration chez la femme enceinte notamment au cours du premier trimestre de la grossesse et chez la femme qui allaite ne doit être envisagé que si nécessaire (cf Sécurité préclinique).
CONDUITE et UTILISATION DE MACHINES
|
Aucune étude sur l’aptitude à conduire des véhicules et à utiliser des machines n’a été réalisée.
Des effets indésirables ont été rapportés chez jusqu’à environ 10 % des patients traités. Ces effets sont fonction de la dose et de la sensibilité individuelle. Les plus fréquemment rapportées sont : dysgueusie (goût désagréable et inhabituel) et réactions locales (irritation buccopharyngée, sensation de brûlure de la langue), tremblements fins (en général au niveau des mains), nausées, hypersudation, agitation, céphalées, sensations de vertiges et crampes musculaires. Ces effets indésirables peuvent régresser en une ou deux semaines avec la poursuite du traitement. Comme avec d’autres traitements inhalés, un bronchospasme peut survenir dans de rares cas, se manifestant par une aggravation des râles sibilants immédiatement après la prise. Pour traiter le bronchospasme paradoxal, il conviendra d’avoir recours à une autre forme de salbutamol ou à un autre bronchodilatateur inhalé à action rapide. Le traitement par Ventilastin Novolizer 100 µg/dose poudre pour inhalation sera immédiatement interrompu, le patient doit être examiné et un traitement différent sera instauré si nécessaire.
Des réactions d’hypersensibilité (telles que rash, urticaire, eczéma, érythème et prurit) ont été observées. De très rares cas d’oedème de Quincke (oedème de la face, des lèvres, des yeux et de la gorge), de bronchospasme, d’hypotension, de collapsus, de thrombopénie et de néphrite ont été rapportés. Une tachycardie, avec éventuellement vasodilatation périphérique, peut être observée. Comme avec d’autres bêta-2 stimulants, des troubles du rythme cardiaque (incluant fibrillation auriculaire, tachycardie supraventriculaire et extrasystoles), des palpitations, un angor et des modifications de la pression artérielle systémique ont été rapportés chez certains patients lors d’un traitement par salbutamol.
Il a été décrit dans la littérature un effet stimulant du salbutamol inhalé sur le système nerveux central, se manifestant par une hyperexcitabilité, une hyperactivité, des troubles du sommeil et des hallucinations. Ces phénomènes ont été principalement observés chez des enfants (jusqu’à 12 ans).
La liste ci-dessous présente les effets indésirables possibles du salbutamol par appareil ou organe et par fréquence.
Très fréquent (> 1/10) ; Fréquent (> 1/100, < 1/10) ; Peu fréquent (> 1/1000, < 1/100) ; Rare (> 1/10 000, < 1/1000) ; Très rare, y compris cas isolés (< 1/10 000).
Troubles hématologiques :
- Très rare : thrombopénie.
-
Troubles du système immunitaire :
- Très rare : réaction d’hypersensibilité.
-
Troubles métaboliques :
- Rare : hypokaliémie, hyperglycémie, augmentation des taux d’insuline, d’acide gras libre, glycérol et corps cétosiques.
-
Troubles psychiatriques :Troubles du système nerveux :
- Fréquent : tremblements fins, vertiges.
-
- Rare : hyperactivité.
-
- Très rare : hyperexcitabilité, troubles du sommeil, hallucinations.
-
Troubles cardiovasculaires :
- Rare : tachycardie, arythmie cardiaque (fibrillation auriculaire, tachycardie supraventriculaire, extrasystole), palpitation, angor, modification de la pression artérielle systémique (augmentation ou diminution).
-
Troubles vasculaires :
- Rare : vasodilatation périphérique.
-
- Très rare : collapsus.
-
Troubles respiratoires, thoraciques et médiastinaux :
- Fréquent : toux.
-
- Rare : bronchospasme paradoxal.
-
Troubles gastro-intestinaux :
- Fréquent : nausée, dysgueusie.
-
Anomalies de la peau et du tissu sous-cutané :
- Fréquent : hypersudation.
-
- Rare : prurit, rash, érythème, urticaire, angioedème.
-
Troubles musculosquelettiques :
- Rare : crampes musculaires.
-
Troubles rénaux :Manifestations générales et locales :
- Fréquent : céphalées, réactions locales, irritation buccopharyngée, sensation de brûlure de la langue.
Un surdosage est peu probable avec Ventilastin Novolizer dans les conditions usuelles d’emploi.
-
Symptômes de surdosage :
- En cas de surdosage, les effets indésirables mentionnés plus haut (cf Effets indésirables) sont rapidement observés avec une sévérité augmentée : tachycardie, palpitations, troubles du rythme, agitation, troubles du sommeil, douleurs thoraciques et tremblements le plus souvent des mains mais pouvant se généraliser au corps entier.
- Des réactions psychotiques ont été occasionnellement observées avec des doses excessives de salbutamol.
- En cas de surdosage en salbutamol, une augmentation du passage du potassium extracellulaire à l’intérieur des cellules entraînant une hypokaliémie peut s’associer à une hyperglycémie, une hyperlipidémie et une hypercétonémie.
-
Conduite à tenir :
-
- Le traitement d’un surdosage en ß-sympathomimétique est essentiellement symptomatique. En cas d’ingestion de quantité importante, envisager un lavage gastrique. L’administration de charbon activé et d’un laxatif peuvent réduire l’absorption digestive du ß-sympathomimétique.
-
- L’administration d’un bêtabloquant cardiosélectif peut être envisagée pour le traitement des troubles cardiaques dus à un surdosage en salbutamol. Néanmoins, il convient d’éviter, dans la mesure du possible, l’utilisation des bêtabloquants chez les sujets ayant des antécédents de bronchospasme. Une surveillance électrocardiographique doit être réalisée chez ces patients.
-
- En cas d’hypotension artérielle importante : remplissage vasculaire (dérivés du plasma).
-
- En cas d’hypokaliémie : surveillance du ionogramme sanguin, apport électrolytique.
-
Classe pharmacothérapeutique : agoniste sélectif bêta-2 adrénergique (code ATC : R03AC02).
Le salbutamol est un agoniste sélectif des récepteurs ß-2 adrénergiques. Il exerce un effet sélectif sur les récepteurs ß-2 bronchiques et aux doses thérapeutiques, il est peu actif sur les récepteurs ß-1 cardiaques. Le salbutamol inhalé stimule les récepteurs ß-2 des muscles lisses bronchiques, entraînant une bronchodilatation rapide, significative en quelques minutes et persistant pendant 4 à 6 heures. Le salbutamol induit une vasodilatation entraînant un effet chronotrope réflexe, et des modifications métaboliques, dont une hypokaliémie.
L’absorption et le métabolisme du salbutamol dans les poumons et les voies digestives sont différents.
Après inhalation, environ 20 à 47 % du principe actif présent dans la dose délivrée atteignent les voies respiratoires profondes ; le restant se dépose dans la bouche et la partie supérieure des voies respiratoires et est dégluti. La fraction déposée au niveau bronchopulmonaire est absorbée dans les tissus pulmonaires et la circulation générale, et n’est pas métabolisée par les poumons. En atteignant la circulation systémique, le salbutamol subit un métabolisme hépatique et est excrété principalement par voie urinaire sous forme de produit inchangé et de sulfate phénolique.
La fraction déglutie d’une dose inhalée est absorbée dans les voies digestives et subit un effet de premier passage important avec transformation en sulfate phénolique. Le produit inchangé et le conjugué sont tous deux excrétés principalement par voie urinaire. La majeure partie d’une dose de salbutamol administrée par voie orale ou intraveineuse ou par inhalation est excrétée en 72 heures. La liaison du salbutamol aux protéines plasmatiques est de l’ordre de 10 %.
Les études précliniques n’ont pas mis en évidence de risque particulier chez l’homme à partir d’études conventionnelles de pharmacologie de sécurité, de toxicité à doses réitérées, de génotoxicité, d’études du potentiel cancérigène et de toxicité sur la reproduction.
Les effets observés lors des études de toxicité étaient liés à l’activité bêta-adrénergique du salbutamol.
CONDITIONS DE CONSERVATION
|
A conserver à une température ne dépassant pas + 30 °C.
Conserver la cartouche dans l’emballage extérieur. En cours d’utilisation, conserver à l’abri de l’humidité.
-
Après première ouverture :
- 6 mois.
-
Dispositif Novolizer :
-
-
En cours d’utilisation :
- 1 an.
- Remarque : le fonctionnement du Novolizer a été validé par des tests portant sur 2000 doses unitaires. En conséquence, un nombre maximal de 10 cartouches de 200 doses peut être utilisé avec le même inhalateur au cours d’une année, avant son remplacement.
MODALITÉS MANIPULATION/ÉLIMINATION
|
Cf Posologie/Mode d’administration.
PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE
|
LISTE I
| AMM | 3400936412026 (2004 rév 11.01.2007) 200 doses + inhalateur. |
| 3400936412194 (2004 rév 11.01.2007) recharge 200 doses. |
| | |
| Prix : | 10.40 euros (200 doses + inhalateur). |
| 8.78 euros (recharge 200 doses). |
| Remb Séc soc à 65 %. Collect. |
MEDA PHARMA
25, bd Amiral-Bruix. 75116 Paris
Tél : 01 56 64 10 70. Fax : 01 56 64 10 80
Liste Des Sections Les Plus Importantes :
Pour plus des conseils sur cette application et developpement de cette dernier contacter avec moi dans ma emaile support@mededuct.com




